pH (পিএইচ) কী? এর মান, গুরুত্ব ও ব্যবহার সম্পর্কে বিস্তারিত
“pH” শব্দটি হাইড্রোজেন আয়নের ঘনত্বের একটি পরিমাপ, একটি দ্রবণের অম্লতা বা ক্ষারত্বের পরিমাণগত পরিমাপ। রসায়নে, pH স্কেল সাধারণত 0 থেকে 14 পর্যন্ত হয়ে থাকে। 25°C এ জলীয় দ্রবণ যার pH 7 এর কম থাকে সেগুলি অম্লীয় হয়, যেখানে 7-এর বেশি pH সহ মৌলিক বা ক্ষারীয় । এই আটিকেলে আমরা Ph নিয়ে আলচনা করবো।
পিএইচ লেভেল কি
পিএইচ (pH) হলো একটি পরিমাপক মান, যা কোনো দ্রবণের অম্লতা (এসিডিক) বা ক্ষারত্ব (বেসিক) নির্দেশ করে। এটি ০ থেকে ১৪ পর্যন্ত একটি স্কেলে প্রকাশ করা হয়।
pH এর পূর্ণরূপ কি
pH-এর পূর্ণরূপ হলো “Potential of Hydrogen” বা “Power of Hydrogen”।
বিশুদ্ধ পানির pH এর মান কত
বিশুদ্ধ পানির pH মান ৭, যা নিরপেক্ষ (Neutral) বলে বিবেচিত হয়।
- pH ৭-এর কম হলে এটি অম্লীয় (Acidic) হয়।
- pH ৭-এর বেশি হলে এটি ক্ষারীয় (Alkaline) হয়।
pH এর গুরুত্ব ও ব্যবহার
pH হলো কোনো দ্রবণে হাইড্রোজেন (H+) আয়নের সক্রিয়তার একটি পরিমাপ, যা দ্রবণের অম্লতা বা ক্ষারীয়তা নির্দেশ করে।
জীবদেহে:
হজম প্রক্রিয়া: পাকস্থলীতে খাদ্য হজমের জন্য প্রয়োজনীয় এনজাইমগুলোর কার্যকারিতা pH-এর উপর নির্ভরশীল।
রক্তের pH: রক্তের pH-এর সঠিক ভারসাম্য মানবদেহের স্বাভাবিক কার্যক্রমের জন্য অত্যাবশ্যক।
কোষীয় কার্যকলাপ: কোষের বিভিন্ন কার্যকলাপ, যেমন – প্রোটিন ও এনজাইমের গঠন এবং কার্যকলাপ pH-এর উপর নির্ভর করে।
কৃষিতে:
মাটির স্বাস্থ্য: মাটির pH উদ্ভিদের পুষ্টি গ্রহণ এবং উদ্ভিদের বৃদ্ধিকে প্রভাবিত করে।
ফসল নির্বাচন: বিভিন্ন ফসলের জন্য মাটির pH-এর প্রয়োজনীয়তা ভিন্ন, তাই pH অনুসারে ফসল নির্বাচন করা গুরুত্বপূর্ণ.
শিল্পকলায়:
রাসায়নিক প্রক্রিয়া: বিভিন্ন শিল্প রাসায়নিক প্রক্রিয়ায় pH নিয়ন্ত্রণ অত্যন্ত গুরুত্বপূর্ণ।
খাবার ও পানীয় শিল্প: খাদ্য ও পানীয়ের গুণমান ও স্থায়িত্বের জন্য pH-এর সঠিক মান বজায় রাখা জরুরি।
বিশুদ্ধ পানির pH এর মান 7 কেন
বিশুদ্ধ পানির pH মান 7 হওয়ার কারণ হলো এটি নিরপেক্ষ (neutral) প্রকৃতির। pH হলো জলের মধ্যে হাইড্রোজেন আয়ন (H⁺) এবং হাইড্রক্সাইড আয়ন (OH⁻) এর ঘনত্বের একটি পরিমাপ।
pH স্কেল 0-14 এর মধ্যে সীমাবদ্ধ কেন
pH স্কেল 0 থেকে 14 এর মধ্যে সীমাবদ্ধ থাকার প্রধান কারণ হলো এটি হাইড্রোজেন আয়নের ঘনত্বের (H⁺) লগারিদমিক স্কেল হিসেবে সংজ্ঞায়িত। এটি মূলত জলের আয়নিক গুণফল (ionic product of water) এর ভিত্তিতে নির্ধারিত হয়।
pH এর কাজ কি
pH এর কাজ হলো একটি দ্রবণের অম্লতা বা ক্ষারত্বের পরিমাপ করা। pH স্কেল ০ থেকে ১৪ এর মধ্যে থাকে, যেখানে:
- pH ৭ এর মানে হলো দ্রবণটি নিউট্রাল, যেমন পানির মতো।
- pH ৭ এর নিচে (০-৬) মানে হলো দ্রবণটি অম্লীয় (acidic), যেমন লেবুর রস বা ভিনেগার।
- pH ৭ এর উপরে (৮-১৪) মানে হলো দ্রবণটি ক্ষারীয় (alkaline), যেমন সোডিয়াম হাইড্রোক্সাইড বা বেকিং সোডা।
বিভিন্ন pH এর মান
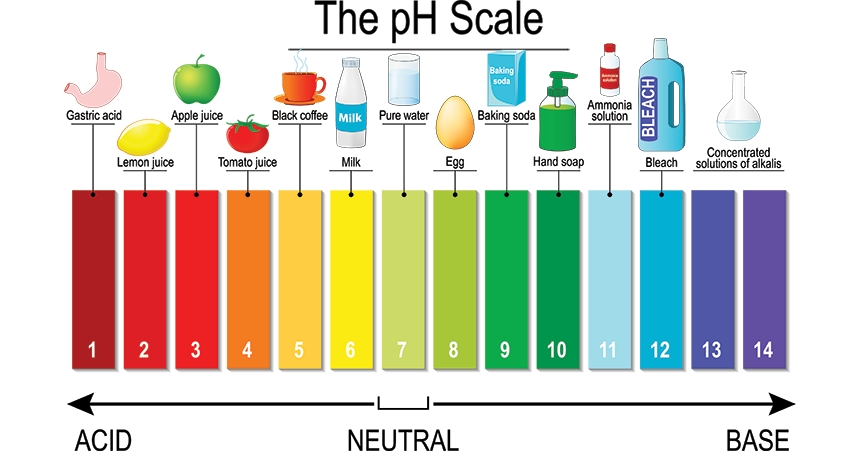
pH স্কেল 0 থেকে 14 পর্যন্ত থাকে, এবং এর মানের উপর ভিত্তি করে একটি দ্রবণের অ্যাসিডিক বা ক্ষারীয় প্রকৃতি নির্ধারণ করা হয়। নিচে বিভিন্ন pH মানের সঙ্গে সম্পর্কিত বিভিন্ন ধরণের দ্রবণের অবস্থান দেওয়া হলো:
pH মান অনুযায়ী দ্রবণের ধরন:
- pH 0 – 3: অত্যন্ত অ্যাসিডিক
- এই pH মানের দ্রবণ খুবই অ্যাসিডিক এবং শক্তিশালী অ্যাসিড যেমন:
- লবণীয় এসিড (যেমন হাইড্রোক্লোরিক এসিড, HCl)
- সালফিউরিক এসিড (H₂SO₄)
- এই pH মানের দ্রবণ খুবই অ্যাসিডিক এবং শক্তিশালী অ্যাসিড যেমন:
- pH 4 – 6: মাঝারি অ্যাসিডিক
- এই pH মানের দ্রবণগুলো মাঝারি অ্যাসিডিক থাকে, যেমন:
- কমলা বা লেবুর রস
- আলু, অ্যাপল বা টমেটো
- দুধ (প্রাকৃতিক কিছু সময়ের জন্য)
- এই pH মানের দ্রবণগুলো মাঝারি অ্যাসিডিক থাকে, যেমন:
- pH 7: নিউট্রাল
- pH 7 একটি নিউট্রাল দ্রবণ, অর্থাৎ neither acidic nor alkaline, যেমন:
- বিশুদ্ধ পানি (H₂O)
- pH 7 একটি নিউট্রাল দ্রবণ, অর্থাৎ neither acidic nor alkaline, যেমন:
- pH 8 – 10: ক্ষারীয় (Alkaline)
- এই pH মানের দ্রবণগুলো ক্ষারীয় থাকে, যেমন:
- সোডিয়াম বাইকার্বোনেট (বেকিং সোডা) দ্রবণ
- তরল সোপ (liquid soap)
- এই pH মানের দ্রবণগুলো ক্ষারীয় থাকে, যেমন:
- pH 11 – 12: মাঝারি ক্ষারীয়
- এই pH মানের দ্রবণগুলো আরও বেশি ক্ষারীয় থাকে, যেমন:
- আমোনিয়া (NH₃) দ্রবণ
- বাড়ির পরিষ্কারের জন্য ব্যবহৃত ক্ষারীয় ক্লিনার
- এই pH মানের দ্রবণগুলো আরও বেশি ক্ষারীয় থাকে, যেমন:
- pH 13 – 14: অত্যন্ত ক্ষারীয় (Strongly alkaline)
- এই pH মানের দ্রবণগুলো খুবই ক্ষারীয় এবং শক্তিশালী ক্ষারীয় দ্রবণ, যেমন:
- সোডিয়াম হাইড্রোক্সাইড (NaOH) বা কস্টিক সোডা
- পটাসিয়াম হাইড্রোক্সাইড (KOH)
- এই pH মানের দ্রবণগুলো খুবই ক্ষারীয় এবং শক্তিশালী ক্ষারীয় দ্রবণ, যেমন:
পানির pH কি
বিশুদ্ধ পানির pH সাধারণত 7। এটি নিউট্রাল হিসেবে গণ্য হয়, কারণ এর মধ্যে হাইড্রোজেন আয়ন (H⁺) এবং হাইড্রোক্সাইড আয়ন (OH⁻) এর পরিমাণ সমান থাকে।
বিশুদ্ধ পানির pH নির্ধারণ:
বিশুদ্ধ পানির মধ্যে স্বতঃস্ফূর্তভাবে (self-ionization) কিছু পরিমাণে হাইড্রোজেন আয়ন (H⁺) এবং হাইড্রোক্সাইড আয়ন (OH⁻) তৈরি হয়
অন্যান্য অবস্থায় পানি:
যখন পানির মধ্যে কোনো দ্রব্য (অ্যাসিড বা ক্ষার) মিশ্রিত হয়, তখন তার pH পরিবর্তিত হতে পারে। উদাহরণস্বরূপ:
- অ্যাসিড যোগ করলে পানির pH 7 এর নিচে চলে আসে (অ্যাসিডিক হয়ে যায়)।
- ক্ষার যোগ করলে পানির pH 7 এর উপরে চলে আসে (ক্ষারীয় হয়ে যায়)।
তবে, বিশুদ্ধ পানি বা ডিস্টিলড পানি তে pH 7 থাকার সম্ভাবনা বেশি।